پرسولفوریک اسید
اسید سولفوریک یا پرسولفوریک اسید همان جوهر گوگرد است که با فرمول شیمیایی H2SO4 می شناسند. این ماده دارای قدرت اسیدی 0.5 است که دارای کاربردهای زیادی در صنعت دارد. در این مقاله به آسنایی با ایمن ماده شیمیایی می پردازیم.

پرسولفوریک اسید چیست؟
این ماده، مایعی است با نقطه جوش بسیار بالا که که مولکول های قطبی آن می توانند به راحتی پیوندهای قوی هیدروژنی با هم برقرار کنند. پرسولفوریک اسید گران روی بالایی دارد و این ویژگی باعث می شود که در آب به راحتی حل شود. در نتیجه محلول های اسیدی مختلفی تولید می کند. این ماده در دسته بندی های مواد معدنی قرار می گیرد. به طور طبیعی این ماده از گازهای خارج شده آتشفشان ها به دست می آید.
این ماده به هر مقداری در آب حل می شود و واکنشی گرمازا را ایجاد می کند. به همین دلیل بهتر است که این ماده را یکباره به آب اضافه نکنیم. به طور کلی این ماده میل ترکیبی زیادی به آب را دارد. پرسولفوریک اسید در هنگام واکنش دادن با دیگر عناصر و مواد، هیدروژن و اکسیژن آنها را با یکدیگر مخلوط می کند سپس به صورت آب از ترکیب جدا می شود. پرسولفوریک اسید ماده اصلی باران های اسیدی است که علت آن ویژگی خورندگی این اسید است.
خواص پرسولفوریک اسید
- این ماده بیرنگ به قهوه ای تیره، روغنی و چگال است. خورنده است و بوی تندی دارد. این نوع اسید بسیار با فلزات واکنش می دهد. هرچه قدر هم که دما بیشتر باشد این واکنش با شدت بیشتری انجام می گیرد.
- استثناء این ماده جیوه و سرب است که بر رروی آنها هیچ گونه تاثیری را ندارد.
- برای استفاده از پرسولفوریک اسید باید تمامی نکات و شرایط ایمنی رعایت شود.
کاربرد پرسولفوریک اسید
همان گونه که بیان شد، اسید سولفوریک از انحلال گاز SO3 در آب قابل استخراج است. روش های دیگر نیز روش های آزمایشگاهی هستند که باید در یک آزمایشگاه کامل و استاندارد تولید شود.
از اسید سولفوریک در تولید ترکیبات شیمیایی استفاده می شود. از اصلی ترین کاربردهایش در تولید کود شیمیایی است. از این ماده در استخراج های مواد شیمیایی کاربردی سنتز عنصرهای شیمیایی و تصویه پس آب های باقی مانده در دبی ها استفاده می شود. از دیگر کاربرد هایش به خاطر خاصیت آبگیری که دارد که در خشک کردن میوه ها کاربرد دارد. اسید سولفوریک کاربردهای متنوع تری هم دارد که در ادامه آنها را بیان می کنیم.
- در تولید مواد نفتی
- تولید ضد یخ و حشره کش ها
- تولید مواد دارویی
- تولید و ساخت پاک کننده های مصنوعی
- استخراج آلومینیوم و مواد آهنی و فولاد
- ساخت و تولید فیلم های عکاسی
- تولید و ساخت دستمال کاغذی
- تولید ابریشم مصنوعی برای تهیه پارچه های ابریشمی
- تولید مواد رنگی
- جداسازی مس از سنگ معدن مس
- مواد منفجره
کاربرد پرسولفوریک اسید در کشاورزی
از مهم ترین استفاده ای که از این ماده می شود در صنعت کشاورزی است. این ماده باعث پایین آوردن PH خاک می شود و گیاهان مواد غذایی بیشتری را از خاک جذب می کنند. در کودهای شیمیایی فسفاته و سولفاته نیز استفاده می شود. در واقع 60% این محصول برای تولید کودهای شیمیایی استفاده می شود. این ماده با واکنش با آهک خاک خنثی می شود. هم چنین این ماده با کربنات هایی که در درون خاک وجود دارد، واکنش می دهد و تولید سولفات کلسیم آبدار می کند.
اثرات اسید سولفوریک در خاک به صورت زیر است:
- کاهش میزان قلیایی بودن خاک و آب
- اصلاح شوری خاک
- بهبود وضعیت تهویه در خاک رسی
- قابلیت تشکیل سولفات های آلی در خاک

خطر پرسولفوریک اسید
با توجه به توضیحات داده شده، پرسولفوریک اسید یک اسید بسیار قوی است که در حین کار با آن باید نکات ایمنی رعایت شود. بدون استفاده از ماسک و دستکش و لباس ایمنی نباید با این ماده در تماس باشید و کار انجام دهید.
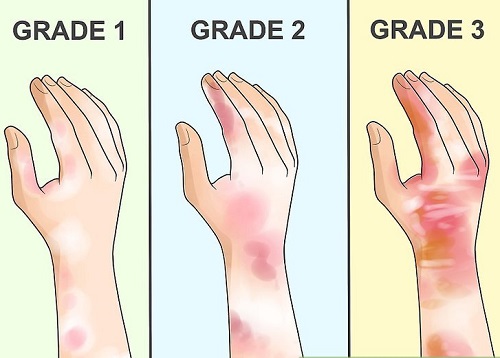
تماس با این اسید می تواند ایجاد سوختگی کند. تماس این ماده با چشم نیز می تواند باعث مشکلات بینایی شود. بهتر است که از استنشاق این ماده جلوگیری شود. استنشاق این ماده می تواند باعث تحریک بینی و حلق و تورم در آن شود.
مضرات اسید سولفوریک
عوارض اسید سولفوریک به صورت مزمن است که ممکن است عوارض بلند مدتی را ایجاد کند و تا سالها باقی بماند. تماس مداوم با این ماده باعث تشدید ریه ها می شود. ممکن است که ریه ها آب بیاورد و برونشیت ایجاد شود. در این صورت، سرفه، خلط و تنگی نفس را همراه دارد. این ماده آسیب شدیدی را به معده و دستگاه تنفسی و دندان ها وارد می کند.

قیمت اسید سولفوریک
پرسولفوریک اسید توسط شرکت های مختلفی تولید می شود که به میزان خلوص و میزان آن تعیین قیمت می شود. با توجه به میزان و حجم اسید نیز تعیین قیمت انجام می شود. بهتر است که برای برآورد هزینه حتما با مشاوران و کارشناسان ما در ارتباط باشید.
سخن آخر
در این مقاله با اسید سولفوریک و خواص ایم متده آشنا شدیم. کاربرد های آن را در انواع صنایع و تولیدات بیان کرده و به نکات ایمنی استفاده از آن نیز پرداختیم. برای خرید این اسد بهتر است که میزان و درصد خلوص اسید را بدانیم و با کارشناسان مربوطه در ارتباط باشیم. با پگاه محیط همرا ه باشید و مقاله اکلیل آلومینیوم را بخوانید.
[faq title=”سوالات متداول پرسولفوریک اسید” open1st=”1″ openAll=”0″][faq_item title=”قیمت اسید سولفوریک چقدر است؟” number=”1″]با توجه به میزان خلوص و میزان آن تعیین قیمت می شود. با توجه به میزان و حجم اسید نیز تعیین قیمت انجام می شود. بهتر است که برای برآورد هزینه حتما با مشاوران و کارشناسان ما در ارتباط باشید.[/faq_item][faq_item title=”اگر اسید سولفوریک را تنفس کنیم چه می شود؟” number=”2″]ممکن است که ریه ها آب بیاورد و برونشیت ایجاد شود. در این صورت، سرفه، خلط و تنگی نفس را همراه دارد. این ماده آسیب شدیدی را به معده و دستگاه تنفسی و دندان ها وارد می کند.
[/faq_item][faq_item title=”مهمترین استفاده ای که از پرسولفوریک اسید می شود چیست؟” number=”3″]از مهم ترین استفاده ای که از این ماده می شود در صنعت کشاورزی است. این ماده باعث پایین آوردن PH خاک می شود و گیاهان مواد غذایی بیشتری را از خاک جذب می کنند. در صنعت کود نیز از این ماده استفاده های فراوانی می شود.[/faq_item][/faq]